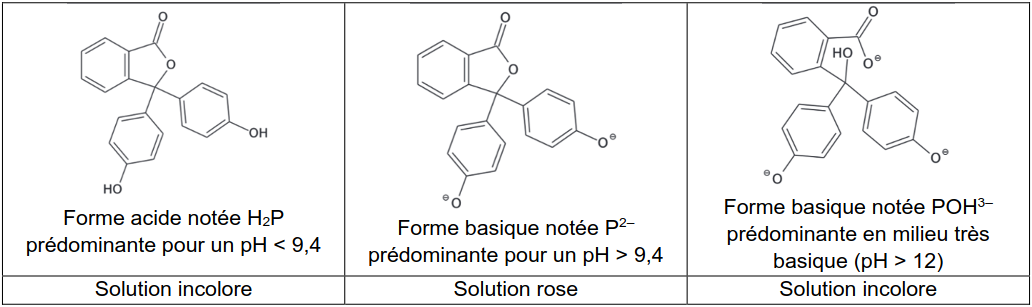
La figure 2 présente l'évolution temporelle de la concentration de la forme \( P^{2-}
\)
de la phénolphtaléine.
{"graphInit": {"range": [[-10, 600], [-0.1, 3]], "scale": [1, 100], "axisArrows": "->", "axisOpacity": 0.5, "gridOpacity": 0.2, "gridStep": [20, 0.1], "tickStep": [1, 1], "labelStep": [5, 5], "unityLabels": true, "xLabel": "Temps en \\( \\:s \\)", "yLabel": "\\(\\left[P^{2-}\\right] \\text{en } 10^{-5}\\:\\text{mol}\\mathord{\\cdot}\\text{L}^{-1}\\)", "yLabelPos": [-0.5, -0.5]}, "path": [[[[-2, 1.4879365079365081], [2, 1.5279365079365081]], {"stroke": "#606060"}], [[[-2, 1.5279365079365081], [2, 1.4879365079365081]], {"stroke": "#606060"}], [[[8, 1.4001211220714862], [12, 1.4401211220714862]], {"stroke": "#606060"}], [[[8, 1.4401211220714862], [12, 1.4001211220714862]], {"stroke": "#606060"}], [[[18, 1.317419706160793], [22, 1.357419706160793]], {"stroke": "#606060"}], [[[18, 1.357419706160793], [22, 1.317419706160793]], {"stroke": "#606060"}], [[[28, 1.2395344457789024], [32, 1.2795344457789024]], {"stroke": "#606060"}], [[[28, 1.2795344457789024], [32, 1.2395344457789024]], {"stroke": "#606060"}], [[[38, 1.166184869862263], [42, 1.206184869862263]], {"stroke": "#606060"}], [[[38, 1.206184869862263], [42, 1.166184869862263]], {"stroke": "#606060"}], [[[48, 1.097106840710527], [52, 1.1371068407105271]], {"stroke": "#606060"}], [[[48, 1.1371068407105271], [52, 1.097106840710527]], {"stroke": "#606060"}], [[[58, 1.032051602805523], [62, 1.0720516028055231]], {"stroke": "#606060"}], [[[58, 1.0720516028055231], [62, 1.032051602805523]], {"stroke": "#606060"}], [[[68, 0.9707848870227047], [72, 1.0107848870227047]], {"stroke": "#606060"}], [[[68, 1.0107848870227047], [72, 0.9707848870227047]], {"stroke": "#606060"}], [[[78, 0.9130860670092601], [82, 0.9530860670092601]], {"stroke": "#606060"}], [[[78, 0.9530860670092601], [82, 0.9130860670092601]], {"stroke": "#606060"}], [[[88, 0.8587473646909368], [92, 0.8987473646909369]], {"stroke": "#606060"}], [[[88, 0.8987473646909369], [92, 0.8587473646909368]], {"stroke": "#606060"}], [[[98, 0.8075731020465478], [102, 0.8475731020465478]], {"stroke": "#606060"}], [[[98, 0.8475731020465478], [102, 0.8075731020465478]], {"stroke": "#606060"}], [[[108, 0.7593789964557369], [112, 0.799378996455737]], {"stroke": "#606060"}], [[[108, 0.799378996455737], [112, 0.7593789964557369]], {"stroke": "#606060"}], [[[118, 0.713991497082497], [122, 0.753991497082497]], {"stroke": "#606060"}], [[[118, 0.753991497082497], [122, 0.713991497082497]], {"stroke": "#606060"}], [[[128, 0.6712471599047022], [132, 0.7112471599047022]], {"stroke": "#606060"}], [[[128, 0.7112471599047022], [132, 0.6712471599047022]], {"stroke": "#606060"}], [[[138, 0.6309920591390885], [142, 0.6709920591390885]], {"stroke": "#606060"}], [[[138, 0.6709920591390885], [142, 0.6309920591390885]], {"stroke": "#606060"}], [[[148, 0.5930812329421733], [152, 0.6330812329421733]], {"stroke": "#606060"}], [[[148, 0.6330812329421733], [152, 0.5930812329421733]], {"stroke": "#606060"}], [[[158, 0.557378161391042], [162, 0.597378161391042]], {"stroke": "#606060"}], [[[158, 0.597378161391042], [162, 0.557378161391042]], {"stroke": "#606060"}], [[[168, 0.5237542748641657], [172, 0.5637542748641657]], {"stroke": "#606060"}], [[[168, 0.5637542748641657], [172, 0.5237542748641657]], {"stroke": "#606060"}], [[[178, 0.49208849105189234], [182, 0.5320884910518924]], {"stroke": "#606060"}], [[[178, 0.5320884910518924], [182, 0.49208849105189234]], {"stroke": "#606060"}], [[[188, 0.4622667789293471], [192, 0.5022667789293471]], {"stroke": "#606060"}], [[[188, 0.5022667789293471], [192, 0.4622667789293471]], {"stroke": "#606060"}], [[[198, 0.43418174812157456], [202, 0.4741817481215746]], {"stroke": "#606060"}], [[[198, 0.4741817481215746], [202, 0.43418174812157456]], {"stroke": "#606060"}], [[[208, 0.40773226218219344], [212, 0.4477322621821935]], {"stroke": "#606060"}], [[[208, 0.4477322621821935], [212, 0.40773226218219344]], {"stroke": "#606060"}], [[[218, 0.3828230743929489], [222, 0.4228230743929489]], {"stroke": "#606060"}], [[[218, 0.4228230743929489], [222, 0.3828230743929489]], {"stroke": "#606060"}], [[[228, 0.35936448477264865], [232, 0.3993644847726487]], {"stroke": "#606060"}], [[[228, 0.3993644847726487], [232, 0.35936448477264865]], {"stroke": "#606060"}], [[[238, 0.3372720170603423], [242, 0.37727201706034236]], {"stroke": "#606060"}], [[[238, 0.37727201706034236], [242, 0.3372720170603423]], {"stroke": "#606060"}], [[[248, 0.31646611450953704], [252, 0.3564661145095371]], {"stroke": "#606060"}], [[[248, 0.3564661145095371], [252, 0.31646611450953704]], {"stroke": "#606060"}], [[[258, 0.29687185339797856], [262, 0.3368718533979786]], {"stroke": "#606060"}], [[[258, 0.3368718533979786], [262, 0.29687185339797856]], {"stroke": "#606060"}], [[[268, 0.2784186732213237], [272, 0.3184186732213237]], {"stroke": "#606060"}], [[[268, 0.3184186732213237], [272, 0.2784186732213237]], {"stroke": "#606060"}], [[[278, 0.2610401225991103], [282, 0.30104012259911034]], {"stroke": "#606060"}], [[[278, 0.30104012259911034], [282, 0.2610401225991103]], {"stroke": "#606060"}], [[[288, 0.24467361997801115], [292, 0.28467361997801116]], {"stroke": "#606060"}], [[[288, 0.28467361997801116], [292, 0.24467361997801115]], {"stroke": "#606060"}], [[[298, 0.22926022827064638], [302, 0.2692602282706464]], {"stroke": "#606060"}], [[[298, 0.2692602282706464], [302, 0.22926022827064638]], {"stroke": "#606060"}], [[[308, 0.2147444426184087], [312, 0.2547444426184087]], {"stroke": "#606060"}], [[[308, 0.2547444426184087], [312, 0.2147444426184087]], {"stroke": "#606060"}], [[[318, 0.2010739905140201], [322, 0.2410739905140201]], {"stroke": "#606060"}], [[[318, 0.2410739905140201], [322, 0.2010739905140201]], {"stroke": "#606060"}], [[[328, 0.18819964356404476], [332, 0.22819964356404474]], {"stroke": "#606060"}], [[[328, 0.22819964356404474], [332, 0.18819964356404476]], {"stroke": "#606060"}], [[[338, 0.1760750402134994], [342, 0.21607504021349938]], {"stroke": "#606060"}], [[[338, 0.21607504021349938], [342, 0.1760750402134994]], {"stroke": "#606060"}], [[[348, 0.16465651879417909], [352, 0.20465651879417907]], {"stroke": "#606060"}], [[[348, 0.20465651879417907], [352, 0.16465651879417909]], {"stroke": "#606060"}], [[[358, 0.1539029602954911], [362, 0.1939029602954911]], {"stroke": "#606060"}], [[[358, 0.1939029602954911], [362, 0.1539029602954911]], {"stroke": "#606060"}], [[[368, 0.1437756402916033], [372, 0.1837756402916033]], {"stroke": "#606060"}], [[[368, 0.1837756402916033], [372, 0.1437756402916033]], {"stroke": "#606060"}], [[[378, 0.13423808949168348], [382, 0.17423808949168346]], {"stroke": "#606060"}], [[[378, 0.17423808949168346], [382, 0.13423808949168348]], {"stroke": "#606060"}], [[[388, 0.12525596241106093], [392, 0.1652559624110609]], {"stroke": "#606060"}], [[[388, 0.1652559624110609], [392, 0.12525596241106093]], {"stroke": "#606060"}], [[[398, 0.11679691369038396], [402, 0.15679691369038395]], {"stroke": "#606060"}], [[[398, 0.15679691369038395], [402, 0.11679691369038396]], {"stroke": "#606060"}], [[[408, 0.10883048161738916], [412, 0.14883048161738915]], {"stroke": "#606060"}], [[[408, 0.14883048161738915], [412, 0.10883048161738916]], {"stroke": "#606060"}], [[[418, 0.10132797843183461], [422, 0.14132797843183462]], {"stroke": "#606060"}], [[[418, 0.14132797843183462], [422, 0.10132797843183461]], {"stroke": "#606060"}], [[[428, 0.09426238701857652], [432, 0.1342623870185765]], {"stroke": "#606060"}], [[[428, 0.1342623870185765], [432, 0.09426238701857652]], {"stroke": "#606060"}], [[[438, 0.08760826361677264], [442, 0.12760826361677263]], {"stroke": "#606060"}], [[[438, 0.12760826361677263], [442, 0.08760826361677264]], {"stroke": "#606060"}], [[[448, 0.08134164619486074], [452, 0.12134164619486075]], {"stroke": "#606060"}], [[[448, 0.12134164619486075], [452, 0.08134164619486074]], {"stroke": "#606060"}], [[[458, 0.07543996816136297], [462, 0.11543996816136298]], {"stroke": "#606060"}], [[[458, 0.11543996816136298], [462, 0.07543996816136297]], {"stroke": "#606060"}], [[[468, 0.06988197710078158], [472, 0.10988197710078158]], {"stroke": "#606060"}], [[[468, 0.10988197710078158], [472, 0.06988197710078158]], {"stroke": "#606060"}], [[[478, 0.06464765824194768], [482, 0.10464765824194769]], {"stroke": "#606060"}], [[[478, 0.10464765824194769], [482, 0.06464765824194768]], {"stroke": "#606060"}], [[[488, 0.05971816238322675], [492, 0.09971816238322675]], {"stroke": "#606060"}], [[[488, 0.09971816238322675], [492, 0.05971816238322675]], {"stroke": "#606060"}], [[[498, 0.05507573801503293], [502, 0.09507573801503294]], {"stroke": "#606060"}], [[[498, 0.09507573801503294], [502, 0.05507573801503293]], {"stroke": "#606060"}], [[[508, 0.050703667395220725], [512, 0.09070366739522073]], {"stroke": "#606060"}], [[[508, 0.09070366739522073], [512, 0.050703667395220725]], {"stroke": "#606060"}], [[[518, 0.046586206347155906], [522, 0.08658620634715591]], {"stroke": "#606060"}], [[[518, 0.08658620634715591], [522, 0.046586206347155906]], {"stroke": "#606060"}], [[[528, 0.04270852756367381], [532, 0.08270852756367382]], {"stroke": "#606060"}], [[[528, 0.08270852756367382], [532, 0.04270852756367381]], {"stroke": "#606060"}], [[[538, 0.03905666721275827], [542, 0.07905666721275828]], {"stroke": "#606060"}], [[[538, 0.07905666721275828], [542, 0.03905666721275827]], {"stroke": "#606060"}], [[[548, 0.03561747465266349], [552, 0.07561747465266348]], {"stroke": "#606060"}], [[[548, 0.07561747465266348], [552, 0.03561747465266349]], {"stroke": "#606060"}], [[[558, 0.03237856507539942], [562, 0.07237856507539943]], {"stroke": "#606060"}], [[[558, 0.07237856507539943], [562, 0.03237856507539942]], {"stroke": "#606060"}], [[[568, 0.02932827490804576], [572, 0.06932827490804576]], {"stroke": "#606060"}], [[[568, 0.06932827490804576], [572, 0.02932827490804576]], {"stroke": "#606060"}], [[[578, 0.026455619811291308], [582, 0.0664556198112913]], {"stroke": "#606060"}], [[[578, 0.0664556198112913], [582, 0.026455619811291308]], {"stroke": "#606060"}], [[[588, 0.023750255123947937], [592, 0.06375025512394794]], {"stroke": "#606060"}], [[[588, 0.06375025512394794], [592, 0.023750255123947937]], {"stroke": "#606060"}]], "plot": [["function(x){ return 0.999199845867464 - 0.00272509048872945 *x;}", [0, 600], {"stroke": "#FF0000"}]]}
6. Déterminer graphiquement à l'aide de la figure 2, la valeur de la vitesse volumique de
disparition \(v_{d}\) de la forme \( P^{2-} \) de la phénolphtaléine à la date \( t = 200 s \).
On donnera un résultat suivi de l'unité qui convient.